|
Seminario
El Ejercicio Actual de la Medicina |
 |
| Cáncer Cérvico Uterino Dr.
José Sanfilippo B |
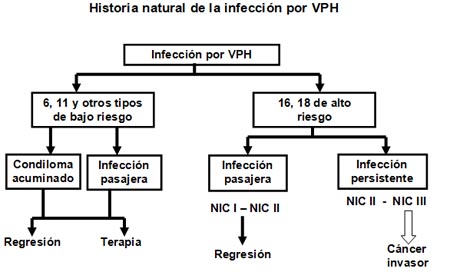
| INTRODUCCIÓN El cáncer cérvico uterino continúa siendo un problema importante de salud pública en el mundo, principalmente en los países en desarrollo. En México, este tipo de cáncer es la primera causa de muerte por neoplasias malignas entre las mujeres de 25 a 64 años. En el 2005, la tasa media nacional de mortalidad fue del 15.46 por 100,000 mujeres de 25 años y más, que corresponde a 4,247 defunciones. El 84% ocurrieron en mujeres con escolaridad primaria o menos y predominantemente en edad productiva. 1 En los últimos años se realizaron investigaciones que han permitido el avance, en el conocimiento de la etiología, diagnóstico y tratamiento del cáncer cérvico uterino, que han impactado en el decremento de las tasas de mortalidad por esta patología. En 1990 la tasa fue de 24.97 y para el 2005 fue de 15.46 por 100,000 mujeres de 25 años y más la disminución fue de 9.51 puntos. Uno de los avances más significativos ha sido la identificación de la etiología del cáncer cérvico uterino, al esclarecer el papel que juega en el desarrollo de las lesiones intraepiteliales el Virus de Papiloma Humano (VPH), ya que se ha detectado hasta en el 99.7% de los carcinomas cervicales2. Los profesores Harold zur Hausen y Lutz Gissman descubrieron entre 1981 y 1984 los VPHs asociados a neoplasias genitales: los tipos 6 y 11 asociados a neoplasias benignas, como el condiloma acuminado y los tipos 16 y 18 asociados al cáncer cervical. Con estos descubrimientos se inició el estudio intenso de los VPhs a nivel mundial y su asociación con esta enfermedad3. En México, los casos de cáncer invasor se encuentran más frecuentemente relacionados con infecciones provocadas por estos dos tipos. Otro de los avances revelantes ha sido el desarrollo de vacunas profilácticas específicas para estos subtipos de virus. La infección por el VPH es transmitida sexualmente y representa la infección de transmisión sexual más frecuente en todo el mundo. En la mayoría de las mujeres, la infección es asintomática y en el 80% de ellas desaparece espontáneamente en un periodo que va entre 12 y 18 meses, debido a una respuesta inmune efectiva, entre otras causas. Sin embargo, es una contradicción que siendo una patología factible de ser detectada en etapas tempranas y tratada de manera oportuna, debido al largo período de tiempo que transcurre entre la aparición de una lesión intraepitelial y su evolución a cáncer, continúen ocurriendo un número importante de fallecimientos. Hablar de la prevención del cáncer cérvico uterino, es complicado debido a que requiere de cambios en el estilo de vida y en el ejercicio de la sexualidad. Prevenir significa modificar o realizar acciones orientadas a evitar o disminuir los factores y cofactores de riesgo que aumentan la posibilidad de contagio. En este contexto, la prevención del cáncer cérvico uterino puede estar enfocada en dos aspectos:
No obstante los avances en este campo, continúa siendo primordial la educación para la salud, la información veraz y oportuna para la población y la promoción de un ejercicio de la sexualidad de manera informada, segura, responsable y libre. Definiciones
ASPECTOS EPIDEMIOLÓGICOS En la mayoría de estos lugares, el número de casos de cáncer invasor se incrementa con la edad, alcanzando la mayor incidencia en las mujeres con edades entre 50 y 60 años. Alrededor del 80-90% de los casos confirmados en países en desarrollo ocurren entre las mujeres de 35 años y más. En México el panorama es similar, la mayor incidencia de casos está en las mujeres con edades entre los 45 y 69 años de edad5. A finales de la década de los años 90s, se investigaba la evidencia epidemiológica de la relación de la infección por VPH y el desarrollo de cáncer cérvico uterino. Entre estas investigaciones se encuentra la realizada por Muñoz y Bosch en 19976. Se menciona que alrededor del 90% de los casos de cáncer cervical pueden estar relacionados con ciertos tipos de virus papiloma humano. Se han identificado más de 50 tipos de VPH que infectan el aparato genital; sin embargo, sólo alrededor de 15 de ellos son considerados altamente oncogénicos o más estrechamente relacionados con el desarrollo de cáncer cérvico uterino: 16, 18, 31, 33, 35, 39, 45, 51, 52, 56, 58, 59, 68, 73 y 82. El análisis de los datos compartidos de 11 estudios de casos y testigos de nueve países, que incluyeron a 1,918 mujeres con cáncer cérvico uterino indicó que tan sólo ocho tipos de VPH contabilizan el 95% de los casos de cáncer cervical (tipos 16, 18, 31, 33, 35,45, 52 y 58)7. Tan solo el VPH 16 estuvo asociado al 50-60% de los casos y el VPH 18, con el 10-12%8. Sin embargo, aún cuando se ha comprobado que la infección persistente por estos tipos de VPH oncogénicos es el principal factor de riesgo para desarrollar cáncer cérvico uterino, se ha demostrado también que la infección persistente es la causa necesaria, pero no la única suficiente para que las lesiones precursoras evolucionen a cáncer9. La infección por VPH es una de las más comunes entre las infecciones de transmisión sexual; no obstante, en la gran mayoría de los casos en los que se presenta, desaparece, regresa o se vuelve indetectable en uno o dos años10. En más del 90% de los casos de cáncer se encuentra presente la infección por VPH, pero no todos los casos de infección por VPH desarrollarán cáncer o incluso lesiones precursoras, ello hace suponer que existen factores que están asociados directa o indirectamente con el aumento en la probabilidad de desarrollar lesiones precursoras o cáncer. Entre los factores que se han identificado se encuentran el tabaquismo, el estado nutricional, la respuesta del sistema inmunológico, la paridad, otras infecciones de transmisión sexual, la inmunosupresión (particularmente en el caso de la infección por VIH). Otros factores como la edad de inicio de vida sexual activa (heterosexual), el número de parejas sexuales, antecedentes de infecciones de transmisión sexual, se les considera en la probabilidad de contraer el VPH, pero no se les considera factores para la evolución de infección por VPH a cáncer11. Recientemente se ha reflexionado acerca de la influencia de otras variables como cofactores en el desarrollo del cáncer cérvico uterino, como la paridad elevada y el uso prolongado de anticonceptivos orales. La investigación realizada por Muñoz, et al12 que comparte datos de ocho casos de estudio y testigos sobre cáncer cérvico uterino y dos de cáncer in situ, en cuatro continentes, sugiere que las mujeres con tres o cuatro embarazos a término presentaban 2,6 veces más alto de desarrollar cáncer que aquellas mujeres nulíparas; en tanto que las mujeres con siete partos o más tenían 3,8 veces mayor riesgo. Otros estudios reafirman esta relación entre alta paridad y cáncer cérvico uterino13,14, aún no se han determinado las razones fisiológicas de esta relación; sin embargo, se ha considerado que los cambios hormonales relacionados con el embarazo y los traumatismos cervicales en el momento del parto pudiesen tener alguna función. Por otro lado, algunas investigaciones como la de Moreno, et al (2002)15 han estudiado la relación potencial entre el uso prolongado de anticonceptivos orales y el desarrollo de cáncer cérvico uterino. El análisis que hicieron estos investigadores de los datos compartidos de diez estudios de casos y testigos de pacientes con cáncer cérvico uterino in situ e invasor, indica que el uso por un plazo prolongado (alrededor de diez años) de anticonceptivos orales aumenta hasta cuatro veces el riesgo de desarrollar cáncer cérvico uterino en las mujeres que tenían además infección por virus papiloma humano. Tomando en consideración estos hallazgos, la Organización Mundial de la Salud convocó a una reunión de expertos en el año 2002 para analizar la relación entre uso de anticonceptivos orales, alta paridad y cáncer cérvico uterino16. El grupo publicó recomendaciones acerca de la manera de prescribir anticonceptivos orales: “Muchos casos de cáncer cérvico uterino pueden prevenirse mediante prácticas de tamizaje apropiadas. Quienes utilizan anticonceptivos orales en lugares en los que se cuenta con servicios de detección deberían recurrir a ellos, tal como se aconseja a otras mujeres. Sin embargo, en muchos entornos se carece de estos servicios; a menudo, los riesgos de morbilidad y mortalidad del embarazo son altos en estos entornos y los anticonceptivos orales combinados son uno de los pocos métodos anticonceptivos ampliamente disponibles. Incluso, dado que la paridad parece ser un factor de riesgo de cáncer cérvico uterino, el uso de los anticonceptivos orales puede reducir el riesgo de cáncer cérvico uterino atribuible a la paridad. No debe negarse a la mujer el uso de anticonceptivos orales combinados simplemente porque la mujer no puede obtener acceso a los servicios de detección. Probablemente, el riesgo de mortalidad materna por la falta de uso de anticonceptivos sobrepasaría ampliamente cualquier riesgo adicional de cáncer cérvico uterino para la mayoría de las mujeres”17. Entre los factores que aumentan la posibilidad de desarrollar lesiones precursoras y cáncer cérvico uterino se encuentra claramente identificado el consumo de tabaco. Algunos estudios indican que las mujeres fumadoras tienen un riesgo de al menos el doble que las mujeres no fumadoras de desarrollar lesiones precursoras y cáncer cervical18,19,20. Las mujeres infectadas por VIH tienen una mayor susceptibilidad de contraer los tipos de VPH altamente oncogénicos, de presentar lesiones precursoras y de manera más rápida que las mujeres seronegativas en el mismo grupo de edad21,22,23. Entre los factores de riesgo que aumentan la probabilidad de desarrollar cáncer cérvico uterino, se encuentran las infecciones concomitantes de VPH y otros agentes de transmisión sexual como la Chlamydia trachomathis y el virus de herpes simple tipo 2 (HSV-2), las mujeres que presentan estas infecciones concomitantes tienen una mayor probabilidad de desarrollarlo que las mujeres sin coinfecciones. De manera particular, se ha estudiado esta relación entre infecciones concomitantes en un análisis de siete estudios de casos y testigos, en él se revisó el efecto de la infección por virus de herpes simple tipo 2 en el desarrollo de cáncer cérvico uterino invasor; se encontró que en las mujeres que fueron seropositivas al ADN de VPH, el HSV-2 presentó una relación de riesgo hasta tres veces mayor de desarrollar cáncer cervical24. Algunos investigadores han planteado que la falta de higiene sea un factor que aumente la probabilidad de riesgo para contraer VPH, desarrollar la infección o de desarrollar cáncer cérvico uterino; sin embargo, estas afirmaciones aún no tienen base sólida25. La infección por VPH es el factor que se encuentra más directamente relacionado con el desarrollo de lesiones precursoras y cáncer cérvico uterino; sin embargo, en sí mismo no es el único determinante, deben estar presentes e interactuar otro tipo de factores como el tipo de virus que esté presente (de los tipos de alto riesgo oncogénico), la carga viral, la respuesta del sistema inmunológico de la mujer, su estado nutricional, si existen otro tipo de infecciones de transmisión sexual concomitantes, si dichas infecciones han sido persistentes. Un porcentaje importante de infecciones por VPH regresa espontáneamente o se mantiene en estado latente durante años, por lo que es importante ser cuidadosos con la información que se maneja respecto a la infección por este tipo de virus, que además es bastante frecuente y común en nuestro país. Uno de los factores sociales que se han retomado en el aumento de probabilidad para desarrollar lesiones precursoras y cáncer es, sin duda, la situación socioeconómica de las mujeres. Una situación socioeconómica baja generalmente está asociada con ingresos económicos precarios, acceso limitado a los servicios de salud, nutrición deficiente y baja escolaridad, con respecto a la prevención de ciertas enfermedades como el cáncer cérvico uterino; además, las prioridades de las mujeres están relacionadas con la satisfacción de necesidades básicas: comida, vivienda, vestido; desafortunadamente, el cuidado de la salud no es una de sus prioridades. Por todo ello, al cáncer cérvico uterino se le relaciona con la pobreza. HISTORIA NATURAL DE LA ENFERMEDAD
DIAGNÓSTICO Las acciones de tamizaje en CaCu están constituidas fundamentalmente por una herramienta básica llamada citología cervical; se trata de un método diagnóstico que permite el examen microscópico directo de las características de las células, del epitelio del cervix y del canal endocervical, utilizando una técnica de tinción conocida como técnica de Papanicolaou. Este método permite realizar un diagnóstico citológico de probable lesión cervical, que es emitido por el citotecnólogo o el patólogo; este diagnóstico incluye desde la ausencia de lesión, pasando por los cambios inflamatorios no patológicos y todo el espectro de displasias leve, moderada y severa, el cáncer in situ y el cáncer invasor. Es importante recalcar que cualquier hallazgo de patología en la citología cervical debe ser confirmado mediante estudio colposcópico y biopsia dirigida27. La citología cervical consiste en tomar una muestra de las células que se descaman del cuello uterino en la zona de transformación. El objetivo principal de la técnica de Papanicolaou es detectar células con alteraciones que indiquen cambios malignos. La importancia de realizarse la citología (Papanicolaou) radica en la enorme posibilidad de detectar de manera temprana lesiones precursoras (displasia leve, moderada o severa) antes de que evolucionen a cáncer, para ser atendidas o para que reciban tratamiento oportuno, de esta forma estaríamos previniendo el desarrollo de casos de cáncer, tomando en cuenta los lapsos de tiempo de evolución que presentan. El resultado citológico que no supone cambio alguno en las células cervicales es el negativo. Uno de los resultados citológicos más frecuentes es el negativo con proceso inflamatorio, que indica que no existen cambios en las células que sean compatibles con alguna de las lesiones precursoras, sino que muestran respuesta del epitelio a inflamación y a cambios regenerativos completamente normales en mujeres con vida sexual activa. Actualmente se reportan los resultados de la citología cervical de acuerdo a la clasificación de Bethesda mencionada en la norma oficial para la Prevención, Detección, Diagnostico, Tratamiento, Control y Vigilancia Epidemiológica del Cáncer Cérvico Uterino. Además existen otros auxiliares de diagnóstico para la detección del cáncer cervicouterino que son procedimientos técnicos cuya finalidad es coadyuvar en la detección de anormalidades de las células o la identificación de lesiones del cuello uterino, siendo complementarios entre sí y son: Visualización cervical con ácido acético, Pruebas de Shiller, Pruebas de biología molecular, Colposcopía e Histopatología. TRATAMIENTO En la mayoría de los casos, las displasias leves deben ser vigiladas más que tratadas, puesto que usualmente desaparecen con el tiempo. En cambio, las displasias moderadas y particularmente las severas, deben ser tratadas ya que un porcentaje significativo de éstas evolucionan a cáncer. Es básico hacer hincapié en las mujeres acerca de la importancia de acudir a la unidad de salud en la que le tomaron la citología cervical, ya que seguramente ahí le indicarán qué hacer de acuerdo al resultado de su estudio. En caso de un resultado con lesión precursora, existen lineamientos de atención y tratamiento, establecidos por la norma oficial. En el caso de las displasias leves, generalmente se mantienen bajo vigilancia en la unidad de salud, debido a que es muy común que tengan una regresión espontánea. Se indica tratamiento y se repite la toma citológica a los seis meses. De acuerdo a la edad de la mujer y a la evolución de la lesión, el médico decide si refiere a clínica de colposcopia o permanece en control en el centro de salud. Si a los seis meses el resultado del Papanicolaou continúa siendo de displasia leve y la mujer tiene una edad de 50 años o más, será referida a la clínica de colposcopia para su valoración; en cambio, si es el mismo resultado y la mujer es menor de 35 años, continuará en control en el centro de salud. Los casos con resultado citológico de infección por VPH, displasia moderada, displasia severa, cáncer in situ y cáncer invasor deberán ser referidos a una Clínica de Colposcopia para su valoración por el médico colposcopista. Este realizará el estudio, diagnóstico colposcópico y definirá el tratamiento. Actualmente se llevan a cabo procedimientos que no requieren hospitalización, que se realizan en consultorio para destruir o remover tejido con lesión. El tratamiento específico dependerá de la severidad, extensión y localización de la lesión o lesiones. Existen dos tipos de procedimientos: el de ablación y el de escisión. El procedimiento de ablación destruye el tejido anormal; el método más utilizado es la crioterapia, que consiste en la aplicación de temperatura inferior a 0º C, que alcanza el punto de congelación en las células produciendo la muerte celular. Es un procedimiento efectivo en un 80 ó 90% en el tratamiento de lesiones de alto grado. La principal desventaja de éste es que no permite la obtención de muestra histológica para su posterior estudio patológico. En cambio, el procedimiento de escisión permite obtener especímenes histológicos. Este es más efectivo para tratar lesiones grandes y lesiones endocervicales. La técnica electroquirúrgica de escisión (LEEP por sus siglas en inglés: Loop Electrosurgical Escisión Procedure) utiliza un asa de alambre eléctrico fino para remover completamente la zona de transformación afectada en el cuello uterino. Este procedimiento es efectivo en un 90 o 95% en el tratamiento de displasias de alto grado. Para los casos de cáncer invasor, éstos son referidos a los centros oncológicos o unidades hospitalarias con unidad de oncología; el tratamiento dependerá del grado de avance del cáncer. Entre los tratamientos se encuentran la histerectomía, la radioterapia y la quimioterapia o una combinación de ellos. Se resalta de nuevo la importancia de la detección temprana, mientras más inicial sea, se tienen mayores probabilidades de éxito con el o los tratamientos. PREVENCIÓN En esta corresponsabilidad corresponde al equipo de salud tener presente que la lesión precursora directa del cáncer cervical es la displasia severa y que esta lesión progresa a cáncer en un período de alrededor de 10 años. Si la lesión es detectada y tratada durante este período, es posible prevenir el desarrollo del cáncer; que la principal razón de una baja incidencia de cáncer en los países desarrollados es que las mujeres son tamizadas de manera regular para detectar lesiones precursoras o precancerosas y que actualmente la técnica de tamizaje para cáncer cérvico uterino más utilizada en el Sector Salud es la citología exfoliativa también conocida como el Papanicolaou (PAP). Si aunado a ello se toma en cuenta que “La citología cervical es una prueba de bajo costo, sencilla y con una alta especificidad (95 %) y sensibilidad (90%) para la enfermedad. Sin embargo, estas características presuponen que el personal que toma la muestra ha recibido el entrenamiento necesario para realizar toma de muestras óptimas para el estudio, por lo tanto, el adiestramiento de la técnica de toma de citología cervical debe estar incluido en las actividades obligadas del personal de salud que se encuentra en formación, especialmente quienes tendrán oportunidad de desarrollarse en el campo asistencial”28. Como ya se mencionó, el cáncer cervicouterino es fácilmente prevenible por lo que la Promoción de las medidas preventivas es la base para reducir su incidencia. Algunas acciones pueden ser:
Asimismo, corresponde a la población en general modificar sus estilos de vida que ponen en riesgo la salud pública y con ello se puede prevenir la incidencia del virus del papiloma humano. Por lo cual se requiere que busquen información acerca de los factores de riesgo y medidas de prevención para evitar el contagio y transmisión del VPH. Y por su parte las mujeres que nunca se han realizado la citología cervical, que hayan iniciado vida sexual, que se encuentren en el grupo de edad de 25 a 64 años, principalmente las de 35 a 64 años, deben practicarse el estudio de tamizaje de Papanicolaou anualmente; sin embargo, se puede practicar si ya se ha iniciado vida sexual, independientemente de la edad.
PRONÓSTICO DISCUSIÓN O COMENTARIO Los conocimientos científicos y tecnológicos están modificándose constantemente prueba de ello es la creación de la vacuna preventiva y terapéutica contra el cáncer cervicouterino que todavía está en la fase de ensayos clínicos, aunque se ha establecido una polémica sobre su uso y efectividad en diversas partes del mundo. Para efectos de este trabajo nos reservamos hablar de ella porque la bibliografía existente aún no es concluyente, por lo que consideramos que podría ser tema para otro trabajo. REFERENCIAS BIBLIOGRÁFICAS
|